Първата галванична клетка в света е разработена от Луиджи Галвани. Прочетете за нейната история. в тази статияПо същество това е временен източник на електрически ток, генериран от химическа реакция. Потокът от електрони се генерира от взаимодействието между два различни метала. В резултат на това химическата енергия се преобразува в електрическа енергия, която след това може да се използва в ежедневието.
Концентрационната галванична клетка е източник на ток, който се състои от два еднакви метални електрода, поставени в смес от соли на този метал в различни концентрации.
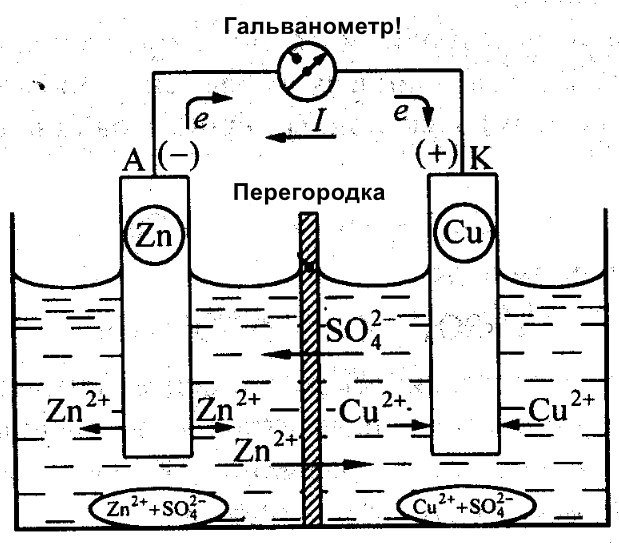
Освен Галвани, Даниел Якоби също е работил върху създаването на ефективна батерия. Той леко е модифицирал своя източник на енергия. Той се състои от медна пластина, поставена в CuSO4, и цинкова пластина, потопена в ZnSO4. За да се предотврати директното им взаимодействие, между тях е поставена пореста стена. По-долу е показана диаграма на галваничния елемент на Даниел Якоби.
Цинкът и медта имат различна реактивност и следователно зарядът им ще се различава. В резултат на това нивата на електродите също не са еднакви. Това им позволява да се движат и да генерират електрически или галваничен ток. Този ток започва да тече, когато човек или изобретателят на устройство за съхранение на ток свърже товар. Този товар може да бъде електрическа крушка, радио, компютърна мишка или други електрически устройства.
Схематична диаграма на галванична клетка
Електрическата схема се отнася до нейния състав и структура. Тя може да бъде изградена от няколко химични елемента с помощта на помощни устройства. По-долу ще бъде описана накратко структурата на галванична клетка. Прочетете повече за това в тази статия.!
Структурата на галванична клетка
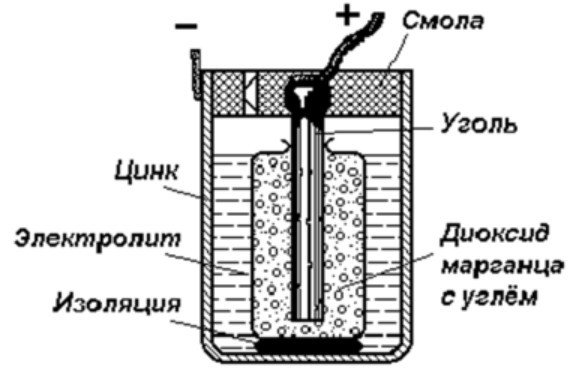
Най-простото устройство за съхранение на енергия се състои от:
- Въглищен прът.
- Два различни метала.
- Електролит.
- Смола или пластмаса.
- Изолатор.
Както може да се види от тази диаграма, галваничната клетка се състои от отрицателен и положителен електрод. Те могат да бъдат направени от мед, цинк или други метали. Те се наричат медно-цинкови клетки. Понякога се наричат сухи батерии.
Обозначение на галванична клетка в диаграма Изработен е под формата на две вертикални линии, разположени близо една до друга на малко разстояние. Едната от тях ще бъде по-малка. В краищата на всяка такава линия има знаци, указващи полярностДългата линия е маркирана като положителна, а късата - като отрицателна. Напрежението може да е показано до нея. Това означава, че веригата, използваща батерията, работи само при това напрежение.
Принципът на действие на галванична клетка
Галваничната клетка работи чрез движението на електрони от един метален контакт към друг. Произтича химическа трансформация. Прочетете повече за термодинамиката на галваничната клетка и образуването на галванично електричество. Тук.
Отговори на често задавани въпроси
| Галваничен | Обяснение |
| Батерия | Източник на енергия, който функционира чрез процеси, протичащи в ограничено, миниатюрно пространство. По-конкретно, енергията се генерира чрез химическа реакция. |
| Волтова клетка или Волтова стълб | Това е енергиен елемент, създаден за първи път от учен на име Волт. |
| Процес | Взаимодействието между химичните елементи, което води до образуването на електрически ток. |
| Изписване | Това е завършването на химическа реакция. Тоест, няма да има взаимодействие между веществата. Галваничният разряд присъства във Warframe. По същество това е модификация, която е в недостиг. Използва се за оръжия за близък бой. ПолярностV2. |
| Галваничен контакт | Това е контактът между електродите и разтвора. |
| Ефект | Появата на разлика между два контакта, направени от два вида метал. Големината зависи от температурата и химичния състав на проводниците. По същество това е първият закон на Волта. |
| Връзка/звено/верига | Свързване на две или повече секции от електрическа верига към източник на ток. |
| Галваничен заряд | Зареждане на батерията с енергия. |
Поцинковането е химичен процес, използващ електрически ток. Реакцията намалява количеството разтворени метални катиони до такава степен, че те в крайна сметка образуват равномерно покритие върху металния електрод. В резултат на това изделието става по-издръжливо, малките вдлъбнатини изчезват и външният му вид става по-привлекателен.
Видове галванични клетки
Има редица специфични видове батерии.
Таблица с галванични клетки
| Тип | Напрежение | Основни предимства |
| Литий | 3 V | Голям капацитет, висок ток. |
| Солни батерии или въглерод-цинк | 1,5 инча | Най-евтиният. |
| Никелов оксихидроксил NiOOH | 1,6 волта | Висок ток. Висок капацитет. |
| Алкални или алкални | 1,6 V | Висок ток. Добър обем. |
Тази тема е разгледана по-подробно в статията. видове батерии!
Предназначение на галванична клетка
Предназначен е за стартиране на електрическо оборудване. Те могат да включват:
- Гледайте.
- Дистанционни управления.
- Фенерчета.
- Медицинско оборудване.
- Лаптопи.
- Играчки.
- Ключодържатели.
- Телефони.
- Лазерни показалки.
- Калкулатори.
И подобни неща около нас.
Галванична клетка у дома
Можете сами да си направите прост източник на захранване. За целта ще ви трябват следните материали:
- Пластмасова чаша.
- Електролит. Това може да бъде физиологичен разтвор, сода или лимонена киселина, разредена във вода.
- Плочи от два различни метала. Например, алуминий и мед.
- Проводници
Производствен процес
Вземете пластмасова чаша и изсипете електролита в нея. Не я пълнете догоре; най-добре е да я оставите 1-2 сантиметра къса. Прикрепете проводниците към металните пластини. След това поставете медните и алуминиевите пластини по краищата на съда. Те трябва да са успоредни една на друга. След като всичко е готово, можете да измерите напрежението с волтметър.
Свържете устройството и докоснете сондите до контактите на нашия източник на захранване. Задръжте ги на място, докато дисплеят покаже напрежение. Обикновено то е 0,5-0,7 волта. Тези стойности зависят от електролита, или по-точно от веществото, използвано като електролит.
Ето как се прави домашно приготвена галванична клетка.